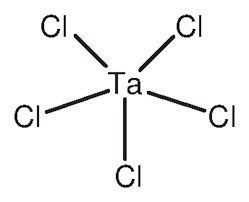
كلوريد التنتالوم، والذي يُطلق عليه غالبًاكلوريد التنتالوم(كلوريد الصوديوم(TaCl₅) مركب أبيض بلوري غير عضوي، يلعب دورًا محوريًا في الصناعات الكيميائية والإلكترونية المتقدمة. في صورته النقية (صيغته TaCl₅)، يكون مسحوقًا أبيض اللون، ويُستخدم كمادة أولية لمجموعة واسعة من المواد الكيميائية القائمة على التنتالوم. يتميز TaCl₅ بتفاعليته العالية، إذ يتحلل بسهولة في الهواء ليشكل أكسيد التنتالوم، وفي النهاية، خماسي أكسيد التنتالوم، لذا يجب التعامل معه دائمًا تحت إشراف طبي.لا مائيظروف خالية من الماء. هذه الحساسية للرطوبة تعني أن TaCl₅ يُخزَّن ويُشحن عادةً في حاويات جافة ومختومة.
في هذه المقالة، نستكشفموضوعين رئيسيينأولاً، الاستخدامات الرئيسية لكلوريد التنتالوم في الصناعة والبحث؛ وثانياً، كيفية إنتاج TaCl₅ واستخلاصه من المواد الخام. ستكون المناقشة متاحةً لغير المتخصصين، مع شرح واضح واقتراحاتٍ حول كيفية استخدام مخطط أو جدول للمساعدة في الفهم. وسنعتمد، قدر الإمكان، على المصادر التقنية لضمان الدقة، بما في ذلك المعلومات من مطبوعات المنتجات المتخصصة.
الاستخدامات الرئيسية لكلوريد التنتالوم
خماسي كلوريد التنتالوم هو مادة كيميائية متعددة الاستخداماتمتوسطومحفز. لأنه قويحمض لويسيُستخدم TaCl₅ (مستقبل أزواج الإلكترونات) في العديد من التفاعلات الصناعية وعمليات المواد. من أهم تطبيقاته:
● المحفز في التركيب العضوي:يعمل TaCl₅ كمحفز محب للإلكترونات، تمامًا مثل كلوريد الألومنيوم (AlCl₃). ويُستخدم لتعزيز التفاعلات المتخصصة، مثل البلمرة أوفريدل-كرافتسالأسيلات والألكلات من النوع. استُخدم كمحفز في تفاعلات تكوين البوليمرات الثلاثية الحلقية لبعض الألكاينات، وفي تحضير مركبات الكلورو-أريلوكسيد.
● مادة أولية لأكاسيد التنتالوم وأوكسيكلوريدات:لأن TaCl₅ يتحلل مائيًا إلى أكسيد التنتالوم (TaOCl₃) ثم إلى خماسي أكسيد التنتالوم (Ta₂O₅)، فإنه يُستخدم بشكل روتيني في تصنيع هذه المواد. يُعد Ta₂O₅ أكسيدًا عازلًا رئيسيًا يُستخدم في المكثفات والطلاءات عالية القيمة. عمليًا، يمكن تحويل TaCl₅ (بإضافة الماء أو الأمونيا) إلى أكاسيد تنتالوم نقية للغاية أو إلى أكسيد كلوريد الأمونيوم الذي يُحرق بعد ذلك إلى أكاسيد. هذا المسار هو أحد أسباب كون TaCl₅ مادة خام أساسية لصناعة التنتالوم.
● ترسيب المواد شبه الموصلة:في صناعة الإلكترونيات الدقيقة، يتم استخدام TaCl₅ كغاز أولي لـالترسيب الكيميائي للبخار (CVD)وترسيب الطبقة الذرية (ALD)من الأغشية الرقيقة المحتوية على التنتالوم. على سبيل المثال، يمكن تفاعل بخار TaCl₅ مع بلازما الأمونيا أو النيتروجين لترسيب أغشية رقيقة من نتريد التنتالوم (TaN)، وهي مادة تُستخدم كحاجز انتشار أو قطب كهربائي في الدوائر المتكاملة. كما تُستخدم لترسيب أغشية خماسي أكسيد التنتالوم للمكثفات. استقراره في بيئات الكلور يجعله مثاليًا لهذه العمليات عالية الحرارة.
● الإلكترونيات والسبائك:في النهاية، يتم تحويل جزء كبير من TaCl₅ المنتج إلىمعدن التنتالومللاستخدام في المكونات الإلكترونية. تعتمد مكثفات التنتالوم - وهي مكثفات صغيرة تُستخدم في الهواتف المحمولة وأجهزة الكمبيوتر المحمولة وغيرها من الأجهزة الإلكترونية - على Ta₂O₅ عالي النقاء (المشتق من TaCl₅) كمادة عازلة. يُعد TaCl₅ بحد ذاته حجر الأساس: إذ يمكن اختزاله (على سبيل المثال باستخدام الصوديوم أو الألومنيوم) لإنتاج مسحوق تنتالوم ناعم، والذي يُستخدم بعد ذلك في صناعة المكثفات والسبائك عالية الحرارة. باختصار، TaCl₅ هوضروري لصنع معدن التنتالوموبالتالي، ينطبق هذا على صناعة مكثفات التنتالوم بأكملها. (قد يساعد جدول أو مخطط انسيابي يلخص عملية تحويل كلوريد التانتالوم₅ إلى معادن وأكسيد ونتريدات القراء على تصور هذه المسارات.)
باختصار، يُستخدم خماسي كلوريد التنتالوم حيثما تكون هناك حاجة إلى مركبات أو أغشية تنتالوم نقية للغاية. فهو يُمكّن من:عمليات الكيمياء العضوية(كمحفز وعامل كلور) وعمليات المواد(ترسيب الأغشية، تخليق الأكاسيد). وفقًا لبيانات الشركة المصنعة، يُستخدم TaCl₅ "كمادة أولية لمركبات عنقودية M₆ ثماني السطوح ذات جسر حافة جديدة"، ويشارك في تصنيع أوكسي كلوريد التنتالوم (V) وخماسي أكسيده. طبيعته المحبة للإلكترونات، المشابهة لطبيعة المحفزات الكلاسيكية مثل AlCl₃، تُبرز دوره في الكيمياء المتقدمة.
كيفية تحضير كلوريد التنتالوم
يتضمن إنتاج خماسي كلوريد التنتالوم كلورة التنتالوم في شكلٍ ما. هناك طريقتان رئيسيتان: كلورة معدن التنتالوم، وكلورة مركبات التنتالوم (عادةً أكاسيد). في جميع الحالات، يجب أن يتم التفاعل في بيئة جافة وخالية من الأكسجين. العمليات الأساسية هي:
● الكلورة المباشرة للتنتالوم المعدني:يُسخّن معدن التنتالوم المُفرّغ بدقة (غالبًا ما يكون برادة أو مسحوقًا) في تيار من غاز الكلور. عند درجات حرارة تتراوح بين 170 و250 درجة مئوية، يتفاعل الكلور مع المعدن لتكوين بخار TaCl₅:
2 Ta+5 Cl2⟶2 TaCl5.2\,Ta + 5\,Cl_2 \longrightarrow 2\,TaCl_5.
هذا التفاعل الطارد للحرارة يُحوّل المعدن بسرعة إلى كلوريد. عمليًا، يُوضع التنتالوم في فرن أو مفاعل، ويُمرّر غاز Cl₂ فوقه عند درجة حرارة مُتحكم بها. ثم يُكثّف بخار TaCl₅ الناتج إلى سائل أو صلب أثناء تبريده. (تستخدم طريقة مشابهة غاز كلوريد الهيدروجين (HCl) بدلًا من Cl₂، لكن هذا يتطلب درجة حرارة أعلى - حوالي 400 درجة مئوية - لبدء التفاعل).
● الكلورة غير المباشرة (من الأكاسيد):غالبًا ما يكون معدن التنتالوم عالي النقاء غير متوفر بسهولة أو باهظ الثمن. بدلًا من ذلك، يمكن البدء بأكسيد التنتالوم الخماسي (Ta₂O₅)، المتوفر بكثرة في مركزات الخام. يمكن تحويل Ta₂O₅ إلى TaCl₅ باستخدام عامل كلورة مثلكلوريد الثيونيل (SOCl₂).التفاعل هو:
Ta2O5+5 SOCl2→240∘C2 TaCl5+5 SO2.\text{Ta}_2\text{O}_5 + 5\,SOCl_2 \xrightarrow{240^\circ\text{C}} 2\,TaCl_5 + 5\,SO_2.
في هذه الطريقة، يُخلط Ta₂O₅ الصلب مع SOCl₂ السائل ويُسخّنان (حوالي ٢٤٠ درجة مئوية). يُحوّل SOCl₂ الأكسيد بفعالية إلى كلوريد، مُنتجًا غاز ثاني أكسيد الكبريت كناتج ثانوي. تُعدّ هذه الطريقة غير المباشرة مفيدة عند العمل مع مساحيق الأكسيد، ويمكن أن تُنتج TaCl₅ نقيًا جدًا.
كلا الطريقتين أعلاه تنتجانغاز TaCl₅، والتي يجب أن تكون بعد ذلكمكثف ومنقىعمليًا، يُبرَّد الغاز المحتوي على الكلور حتى يسيل كلوريد TaCl₅ (درجة غليانه حوالي ٢٣٩ درجة مئوية). يُستخدم التقطير غالبًا لفصل كلوريد TaCl₅ عن أي شوائب أو مواد ذات درجة غليان منخفضة. على سبيل المثال، عند التحضير في المختبر، قد يُمرَّر الغاز عبر مصيدة باردة أو سلسلة من المكثفات. بعد التكثيف، يُجفف المنتج (يُسخَّن برفق تحت التفريغ) لإزالة آثار الرطوبة. ينتج عن ذلك مادة صلبة بيضاء عالية النقاء. (أطاولةإن تلخيص طرق التركيب هذه - سرد المتفاعلات والظروف والمنتجات - قد يساعد في مقارنة الطرق جنبًا إلى جنب.
● الاستخلاص الصناعي من الخام:على نطاق واسع، يُستخرج التنتالوم غالبًا من معادن مثل التنتاليت أو الكولتان، والتي تحتوي على كلٍّ من أكاسيد التنتالوم والنيوبيوم. في إحدى العمليات الصناعية، يُمزج مُركّز الخام مع الكربون (فحم الكوك) ويُتفاعل مع غاز الكلور عند درجة حرارة عالية. تُحوّل هذه الكلورة الكربوكسيلية الأكاسيد إلى كلوريدات متطايرة. في البداية، يتكوّن خليط من كلوريدات التيتانيوم والنيوبيوم والتنتالوم ويتكثّف ليُشكّل سائلًا يُسمّى "أوكسيد كلوريد التيتانيوم - النيوبيوم - التنتالوم". يُقطّر هذا السائل تقطيرًا جزئيًا: يُزال أولًا رباعي كلوريد التيتانيوم (TiCl₄) (عند الغليان عند درجة حرارة 136 درجة مئوية)، تاركًا معظم كلوريدات النيوبيوم والتنتالوم. ثم يُكرّر الخليط المتبقي (عند الحاجة) لتحويل أيّ أوكسي كلوريد إلى خماسي كلوريد. أخيرًا، يُفصل كلوريد النيوبيوم (NbCl₅) وكلوريد التنتالوم (TaCl₅) بالتقطير التجزيئي، حيث يغلي TaCl₅ عند 239 درجة مئوية وNbCl₅ عند 248 درجة مئوية. والنتيجة النهائية هي TaCl₅ نقي. غالبًا ما يُتفاعل TaCl₅ هذا مع الأمونيا المائية لترسيب فلوريد التنتالوم الأمونيوم أو أوكسي كلوريد، والذي يُنتج عند التكليس Ta₂O₅ فائق النقاء. في جوهره، يُستخدم TaCl₅ كوسيط في تنقية التنتالوم من خاماته.مخطط انسيابيإن توضيح هذه الخطوات - من الخام إلى TaCl₅ إلى الأكسيد - سيكون مفيدًا للقراء لتصور العملية الصناعية.
باختصار، يُنتَج كلوريد التنتالوم عن طريق هالوجينة معدن التنتالوم أو مركباته. تُعدّ الكلورة المباشرة لمعدن التانتالوم باستخدام Cl₂ أبسط الطرق المخبرية، بينما غالبًا ما تستخدم العمليات الصناعية كلورة عالية الحرارة لمركزات أكسيد التنتالوم باستخدام الكربون (الكلورة الكربونية) أو مع عوامل كلورة أخرى. يُكثَّف بعد ذلك غاز TaCl₅ ويُقطَّر إلى درجة نقاء عالية. يُشار إلى أن إحدى المذكرة الفنية لأحد المصنّعين تُؤكِّد على استخدام TaCl₅ في "كلورة المواد العضوية" و"كوسيط كيميائي" في إنتاج معدن التنتالوم النقي، مما يُؤكِّد دوره ككاشف ووسيط رئيسي.


ملخص
كلوريد التنتالوم(TaCl₅) هو وسيط كيميائي رئيسي في صناعة التنتالوم. ويُستخدم على نطاق واسع كـالمواد الأوليةلصنع مركبات التنتالوم الأخرى (أكاسيد، نيتريدات، معادن) ويعمل كـمحفز حمض لويسفي التفاعلات الكيميائية المتخصصة. تتراوح التطبيقات الشائعة من الإلكترونيات (مكثفات التنتالوم، والأغشية الرقيقة لأشباه الموصلات) إلى التركيب العضوي المتقدم. ولأن TaCl₅ حساس للرطوبة ومسبب للتآكل، فإن التعامل معه يتطلب ظروف جفاف صارمة.
يتضمن إنتاج TaCl₅ كلورة التنتالوم بشكل أو بآخر. في المختبر، يعني هذا تفاعل معدن أو أكسيد Ta مع الكلور (أو مصادر الكلور). أما في الصناعة، فيعني ذلك استخدام كلورة عالية الحرارة لمركزات الخام، غالبًا باستخدام الكربون، يليها التقطير. تتطلب جميع الطرق تنقية دقيقة لعزل TaCl₅ النقي وإزالة النواتج الثانوية.
فهم كل منالاستخداماتوطرق الإنتاجيُعدّ فهم كلوريد التنتالوم أمرًا أساسيًا لتقدير دوره في التكنولوجيا الحديثة. من خلال دمج تفاصيل التركيب الكيميائي مع التطبيقات العملية (وتوفير وسائل مساعدة بصرية عند الحاجة)، يمكن للقراء أن يدركوا كيف أن هذا المركب الذي يبدو غامضًا هو في الواقع ركيزة أساسية للمواد القائمة على التنتالوم في الإلكترونيات والكيمياء وغيرها.
وقت النشر: 30 مايو 2025